
新目录
下载我们的洁净室目录
下载大麻提取和成品GMP设备
由于缺乏全球公认的指导方针,FDA尚未在美国大麻行业实施GMP,少数持牌大麻生产商正在建设最先进的GMP设施,以加强他们在美国和加拿大的地位和品牌,并促进GMP认证产品出口到欧洲和澳大利亚。
由于全国大麻娱乐用途合法化,许多加拿大大麻公司很早就进入市场。加拿大许可的大麻公司必须遵守加拿大特定的良好生产规范(GPP)标准,该标准被认为是低于欧盟gmp的质量保证水平。

美国市场仍在以州为单位运作。由于大麻是一个相当新的市场,在美国全国范围内都不合法,联邦机构还没有制定标准。FDA为广泛的产品建立了良好生产规范(GMP)法规,包括食品、人药和兽药、疫苗、医疗设备、辐射电子产品、化妆品、膳食补充剂和烟草产品。显然,大麻几乎可以用于所有这些类别。FDA管辖下的公司被要求遵守最新的法规,通常被称为cGMP,它代表现行良好生产规范.
即使FDA没有指导方针然而,对于大麻相关产品,一些公司正在付出额外的努力,以确保在法规到位时,他们已经准备好并领先于竞争对手。在未来的岁月里,为了保障人民的安全,规章制度将不可避免。要想成为这个行业的先驱,并从一开始就设定更高的客户标准,一个积极主动的方法是遵循一些受监管行业的良好实践,如制药和药物合成行业。
什么是cGMP?
FDA通过仔细监测药品制造商遵守其现行良好生产规范(CGMP)法规的情况来确保药品的质量。药品CGMP法规包含药品生产、加工和包装中使用的方法、设施和控制的最低要求。这些规定确保产品的使用是安全的,并且它具有它所声称的成分和强度。
对于那些想要出口到欧洲和澳大利亚的生产商来说,已经有了严格的规定。良好生产规范(GMP)认证是有国际雄心的医用大麻公司的关键。
GMP标准在最初启动工厂时实施成本更高,但进入国际市场可能会大幅提高投资回报。
计划出口到澳大利亚(TGA-GMP认证)和欧洲(EU-GMP认证)的公司都需要GMP。
虽然娱乐性大麻法规仍然有点模糊,但对于药用产品活性药物成分(API)制造商的药物质量成分来说,情况并非如此。
一些适用的规定
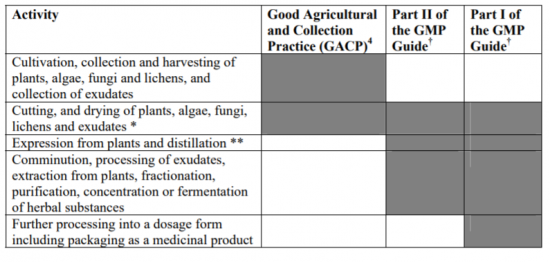
说明良好规范在草药产品生产中的应用的表格
从EU GMP附录7:草药产品的生产
如EU GMP附录7右表所示,对于草药产品的生产,GMP从切割和干燥步骤开始适用。
“草药的GMP分类取决于生产许可持有人对其的使用。该材料可分为活性物质、中间体或成品。药品制造商有责任确保适用适当的GMP分类。”
免责声明
请注意,本页上的信息仅供教育用途。为了帮助理解,定义和概念被过分简化了。如果在这方面需要帮助,请在您的特定流程中寻求专家的建议,并参考适用的法规。